研究人员开发了一种新型化学发光测定法来研究对程序性细胞死亡蛋白1阻断疗法的反应
癌症是一种普遍的疾病,细胞不受控制地分裂和生长,最终扩散到身体的其他区域或器官。非小细胞肺癌(NSCLC)是一种非常流行的肺癌形式。目前针对NSCLC 的治疗策略包括使用免疫检查点抑制剂 (ICIs),因为它们为 NSCLC 患者提供了显着的临床益处。
ICI 针对特定的免疫检查点蛋白,例如细胞毒性 T 淋巴细胞相关蛋白 4 (CTLA-4) 和/或程序性细胞死亡 1 (PD-1)。肿瘤组织中PD-1配体(PD-L1)的表达(tPD-L1)目前被用作确定PD-1或PD-L1靶向治疗对NSCLC患者疗效的生物标志物。然而,由于tPD-L1表达的异质性和预测价值不足,需要额外的生物标志物。
在此背景下,近代大学医学院肿瘤内科学系的 Hidetoshi Hayashi 教授和 Kazuhiko Nakakawa 教授以及免疫学和基因组医学系的 Kenji Chamoto 教授和 Tasuku Honjo 教授组成的日本研究小组,京都大学医学研究生院试图研究血浆中免疫检查点因子的可溶形式,通过基于化学发光磁性技术的自动测定进行测量。他们的研究结果于 2024 年 4 月 1 日发表在《临床研究杂志》上。
Hayashi 教授分享了他们的研究背后的灵感,他说:“诺贝尔医学奖获得者 Honjo 教授认为,使用血液样本而不是肿瘤组织来更动态地了解肿瘤免疫环境非常重要。”
研究小组在PD-1/PD-L1阻断治疗前评估了晚期NSCLC患者血液样本中免疫检查点分子PD-L1、PD-1和CTLA-4的可溶形式。他们对 50 名接受纳武单抗治疗的患者进行了一项前瞻性试验,被称为“发现队列”。接受PD-1/PD-L1阻断治疗、细胞毒化疗或靶向治疗等特定治疗的患者被分为不同的研究队列,统称为“验证队列”并进行回顾性分析。他们发现免疫反应性肿瘤患者的可溶性免疫检查点因子浓度升高,而这些患者对 PD-1/PD-L1 阻断疗法无反应。相反,在接受细胞毒性化疗或靶向治疗的患者中没有发现这种相关性。
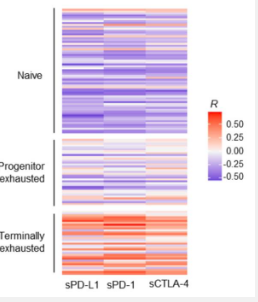
此外,对肿瘤大小、tPD-L1水平以及肿瘤组织和外周CD8 + T细胞中基因表达的综合分析表明,高水平的可溶性PD-L1、PD-1和CTLA-4与抗肿瘤免疫衰竭相关。 。可溶性 PD-L1 和 CTLA-4 水平一起能够有效预测患有热肿瘤(以各种浸润性免疫细胞高度浸润为特征的肿瘤)的 NSCLC 患者中 PD-1/PD-L1 阻断治疗的疗效。
“基于血液的可溶性标记物可以以侵入性较小的方式识别出哪些患者将从 ICI 中获益更多,同时在疗效出乎意料的情况下可能提供另一种治疗选择。此外,对晚期 NSCLC 患者进行适当的选择性治疗将延长生存率,” Hayashi 教授强调,并强调了他们的研究工作在现实生活中的潜在应用。
因此,血浆中可溶性免疫检查点分子作为生物标志物的鉴定可以为晚期非小细胞肺癌患者更好的治疗结果铺平道路。
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
